ผู้ช่วยศาสตราจารย์ ดร.วรวิทย์ จันทร์สุวรรณ
ปรับปรุงล่าสุด: 1 มีนาคม 2564

บทนำ
การตรวจสอบความใช้ได้ของวิธีทดสอบ (method validation) เป็นส่วนที่สำคัญอย่างยิ่งของการพัฒนาหรือปรับปรุงวิธีวิเคราะห์ขึ้นมาใหม่ ซึ่งการตรวจสอบความใช้ได้ของวิธีนั้นเกี่ยวข้องกับแนวทางการออกแบบวิธีการทดลองเพื่อยืนยันหรือพิสูจน์วิธีวิเคราะห์นั้น ๆ มีความเชื่อมั่นเพียงพอที่จะทำให้ได้ผลลัพธ์ที่ถูกต้องภายในขอบเขตการใช้งานที่ต้องการได้ ดังนั้นผู้วิเคราะห์ต้องทำความเข้าใจหลักการพื้นฐานของกระบวนการวิเคราะห์ และข้อจำกัดของวิธีการทดสอบแต่ละวิธี ซึ่งผลลัพธ์จากการตรวจสอบความใช้ได้ของวิธี สามารถใช้ประเมินผลที่เกี่ยวข้องกับความน่าเชื่อถือและความสอดคล้องของผลการวิเคราะห์ หากวิธีการตรวจสอบความใช้ได้ยังไม่ได้ดำเนินการหรือดำเนินการในลักษณะที่ไม่เพียงพอ วิธีวิเคราะห์นั้นจะไม่ได้รับการยืนยันถึงผลลัพธ์ที่ได้ว่ามีความน่าเชื่อถือเพียงพอโดยสิ่งที่สำคัญของการตรวจสอบความใช้ได้ของวิธี คือการกำหนดขอบเขตของวิธีการตรวจสอบซึ่งจะเป็นการกำหนดพารามิเตอร์ (คุณสมบัติ เงื่อนไข หรือข้อจำกัดของวิธีการ) ที่จะต้องประเมินและตรวจสอบในระหว่างการดำเนินการวิเคราะห์ โดยทั่วไปแล้ว ข้อมูลที่ได้จากวิธีวิเคราะห์ที่ไม่ได้รับความน่าเชื่อถือนั้นมาจากการใช้วิธีที่ไม่ผ่านการตรวจสอบความใช้ได้ หรือการตรวจสอบความใช้ได้ของวิธีไม่เพียงพอหรือเหมาะสมสำหรับการวิเคราะห์ตัวอย่างนั้น ๆ (Bridwell et al., 2010, Chauhan, Mittu, & Chauhan, 2015)
โดยทั่วไปวิธีวิเคราะห์ที่ดำเนินอย่างประจำ (routine analysis) หรือวิธีวิเคราะห์ที่เงื่อนไข (condition) เปลี่ยนไป หรือวิธีวิเคราะห์ที่มีการเปลี่ยนแปลงวิธีการ ขั้นตอน โดยที่การเปลี่ยนแปลงอยู่นอกขอบเขตเดิม ซึ่งการดำเนินการวิเคราะห์ในวิธีดังกล่าวจะต้องมีการตรวจสอบความใช้ได้ของวิธี (method validation) และการทวนสอบวิธี (method verification) เสมอ
- การตรวจสอบความใช้ได้ของวิธีทดสอบ (method validation) หมายถึง “การยืนยันโดยการตรวจสอบและจัดทำหลักฐานที่เป็นรูปธรรม เพื่อแสดงว่าข้อกำหนดพิเศษต่าง ๆ สำหรับการใช้ตามที่ตั้งใจไว้โดยเฉพาะสามารถบรรลุผลได้ครบถ้วน” (ISO/IEC 17025:2017)
- การทวนสอบวิธี (method verification) หมายถึง “การทดสอบเพื่อที่จะประกันว่าวิธีการวิเคราะห์มาตรฐานหรือวิธีการวิเคราะห์อ้างอิงที่จะนำมาใช้ในห้องปฏิบัติการมีความถูกต้อง และความเที่ยงเป็นไปตามคุณสมบัติที่กล่าวไว้ของวิธีวิเคราะห์นั้น ๆ” การทวนสอบวิธีเป็นการทวนสอบเพื่อประกันว่าวิธีการวิเคราะห์มาตรฐานหรือวิธีการวิเคราะห์อ้างอิง โดยทั่วไปการทวนสอบวิธีจะเป็นส่วนหนึ่งของการตรวจสอบความใช้ได้ของวิธี
ดังนั้น ทั้งการตรวจสอบความใช้ได้ของวิธีทดสอบ และการทวนสอบวิธีจะเป็นการควบคุมคุณภาพ (routine quality control) ของผลการทดสอบในระหว่างการทดสอบ เพื่อให้แน่ใจว่าการทดสอบมีความแม่น ความเที่ยง และมีความน่าเชื่อถือ โดยทั่วไป การตรวจสอบความใช้ได้ของวิธีจะประกอบด้วยกระบวนการตรวจสอบเพื่อประเมินดังนี้
- วิธีทดสอบที่ใช้ให้ผลตอบสนองต่อสารสนใจทดสอบอย่างไร
- วิธีทดสอบที่ใช้นั้นสามารถให้ผลการทดสอบที่ใกล้ค่าจริงหรือค่าความแม่น (trueness) ขีดจำกัดการตรวจวัด (detection limits) และ ความคลาดเคลื่อน (uncertainty) ตามที่ต้องการ
- ความสัมพันธ์ของปริมาณสารกับการตอบสนองของเครื่องมือเป็นแบบเชิงเส้น
- จะบอกให้ทราบว่าวิธีทดสอบจะตอบสนองต่อตัวอย่างอย่างไรภายใต้สภาวะการทดลองและเครื่องมือที่มีอยู่
- วิธีทดสอบที่เลือกใช้นั้นไม่จำเป็นต้องเป็นวิธีที่ให้ผลการทดสอบที่ดีที่สุด แต่จะต้องให้ผลการทดสอบที่ตรงตามวัตถุประสงค์การใช้งาน
หากมีคำถามว่า สถานการณ์ใดบ้างที่เราจะต้องทำการตรวจสอบความใช้ได้ของวิธีและควรทำในระดับใด คำตอบนี้อาจตอบให้เฉพาะเจาะจงลงไปได้ยาก อย่างไรก็ตามผู้วิเคราะห์ต้องประเมินสถานการณ์ใดในวิธีทดสอบที่อาจก่อให้เกิดความคลาดเคลื่อนหรือความไม่แน่นอนของข้อมูลที่จะได้รับนั้นเสมอ เช่น
- วิธีการทดสอบที่ไม่ใช่วิธีมาตรฐาน (non-standard method) เป็นวิธีที่ยังไม่ได้รับการยอมรับทั่วไป เช่น วิธีที่ห้องปฏิบัติการพัฒนาเอง หรือวิธีที่ห้องปฏิบัติการปรับเปลี่ยน หรือดัดแปลงจากวิธีมาตรฐานอาทิ เปลี่ยนสารเคมีที่ใช้ เปลี่ยนวิธีการย่อยตัวอย่าง หรือเปลี่ยนสภาวะทดสอบ เป็นต้น เมื่อห้องปฏิบัติการนำมาใช้ จะต้องตรวจสอบความใช้ได้ของวิธีเพื่อให้สอดคล้องตามวัตถุประสงค์การใช้งาน
- วิธีการทดสอบที่พัฒนาขึ้นใหม่
- การใช้วิธีมาตรฐานแต่ใช้นอกขอบเขตที่กำหนด
- การใช้วิธีมาตรฐานแต่ทำการปรับปรุง ดัดแปลง หรือขยายขอบเขต นำไปใช้ต่างห้องปฏิบัติการ หรือต่างเครื่องมือวิเคราะห์
- เมื่อมีการเปลี่ยนแปลงวิธีทดสอบที่ไม่ใช่วิธีมาตรฐานที่ได้ผ่านการตรวจสอบความใช้ได้ของวิธี แล้ว
- เมื่อมีการขยายขอบเขตของวิธี เช่น วิเคราะห์สารตัวใหม่ สารที่ระดับความเข้มข้นน้อย ๆ (trace) หรือใช้ปริมาณตัวอย่างน้อยมาก ๆ เป็นต้น
- มีการเปลี่ยนแปลงเครื่องมือวิเคราะห์หลัก
- เมื่อนำวิธีทดสอบเก่า ๆ ที่ได้รับการตรวจสอบความใช้ได้มาใช้อีกครั้ง
- วิธีทดสอบนั้น ๆ ได้ถูกนำไปใช้ในห้องปฏิบัติการอื่น นักวิเคราะห์คนอื่น หรือเครื่องมือที่ใช้แตกต่างออกไปจากเดิม
- เมื่อตัวชี้บ่งการควบคุมคุณภาพของห้องปฏิบัติการ แสดงค่าให้เห็นว่าวิธีทดสอบมีการเปลี่ยนแปลงจากเดิม
- ต้องการเปรียบเทียบความแม่นของวิธีสองวิธีไม่แตกต่างกัน
กรณีที่ห้องปฏิบัติการใช้วิธีทดสอบมาตรฐาน ห้องปฏิบัติการต้องมีข้อมูลยืนยันว่าผลการทดสอบที่ได้มีความแม่นเป็นไปตามที่กำหนดในวิธีมาตรฐานหรือไม่ ทั้งนี้ ข้อมูลที่ใช้ยืนยันจะพิจารณาตามความเหมาะสมในแต่ละวิธีการทดสอบ โดยสรุปคือ ห้องปฏิบัติการสามารถยืนยันผลโดยการทวนสอบวิธี และไม่ต้องจัดทำรายงานแบบฉบับเต็ม
นิยาม
คำว่า การตรวจสอบความใช้ได้ (validation) ได้กำหนดไว้ใน 3 หน่วยงานคือ ISO 9000, ISO/IEC17025 และ VIM (International vocabulary of metrology) ดังนี้ (Magnusson et al., 2014)
- ISO 9000 กำหนดไว้ว่า “confirmation, through the provision of objective evidence, that the requirements for a specific intended use or application have been fulfilled”
- ISO/IEC17025 กำหนดไว้ว่า “confirmation by examination and provision of objective evidence that the particular requirements for a specific intended use are fulfilled”
- VIM กำหนดไว้ว่า “verification, where the specified requirements are adequate for an intended use”
หน่วยงาน The International Council for Harmonization of Technical Requirements for Pharmaceuticals for Human Use (ICH) ได้กำหนดแนวทางและข้อแนะนำเกี่ยวกับคุณลักษณะเฉพาะที่แสดงคุณสมบัติของวิธี (method performance characteristics) หรืออาจเรียกว่าพารามิเตอร์ (parameters) ของการทดสอบความใช้ได้สำหรับวิธีวิเคราะห์แต่ละประเภท โดยกำหนดนิยามคำศัพท์สากลไว้ใน ICH Guideline Q2(R1) “Validation of Analytical Procedures: Text and Methodology” โดยวิธีวิเคราะห์ที่ต้องทำการตรวจสอบความใช้ได้ของวิธี แบ่งเป็น 3 ประเภทคือ
1) การพิสูจน์เอกลักษณ์ (identification tests)
2) การควบคุมสารปนเปื้อน (control of impurities)
2.1) Quantitative tests for impurities content หมายถึง การทดสอบธาตุปริมาณต่ำ การทดสอบประเภทนี้ ห้องปฏิบัติการต้องตรวจสอบหาค่าขีดจำกัดของการวัดเชิงปริมาณ (LOQ) โดยมีหลักฐานเป็นรูปธรรมที่แสดงว่าปริมาณต่ำสุดเท่าไรที่ห้องปฏิบัติการสามารถทดสอบได้ โดยมีความแม่น (accuracy) และความเที่ยง (precision) เป็นที่ยอมรับ
2.2) Limit tests for the control of impurities หมายถึง การทดสอบธาตุปริมาณต่ำมากๆ ซึ่งอาจมีหรือไม่มีธาตุนั้นในตัวอย่างก็ได้ การรายงานผลคือตรวจพบหรือตรวจไม่พบ การทดสอบประเภทนี้ต้องหาขีดจำกัดของการตรวจวัด (LOD)
3) การวิเคราะห์ปริมาณตัวยาสำคัญ (assay) ในยาหรือผลิตภัณฑ์ทางยา หมายถึงการทดสอบธาตุที่มีปริมาณความเข้มข้นสูงในตัวอย่าง ซึ่งห้องปฏิบัติการต้องตรวจสอบว่าความเข้มข้นที่สามารถทดสอบได้อยู่ระหว่างเท่าไร การทดสอบประเภทนี้ไม่จำเป็นต้องหา LOD และ LOQ
ประเภทของการทดสอบ แบ่งประเภทได้เป็น 2 วิธี ดังนี้
- จำแนกตามลักษณะวิธีทดสอบ ซึ่งแบ่งเป็น 2 ประเภทย่อย ดังนี้
1.1 Defining method หรือ Empirical method หมายถึง วิธีทดสอบที่ผลการทดสอบขึ้นอยู่กับวิธีการที่กำหนดในวิธีทดสอบนั้น และผลทดสอบสามารถสอบกลับได้ไปยังวิธีการทดสอบที่ใช้ ดังนั้น วิธีทดสอบนี้ห้ามดัดแปลงวิธี ต้องทำตามวิธีที่กำหนด เช่น การทดสอบหาความชื้นในตัวอย่าง เป็นต้น
1.2 Non-defining method หรือ Rational method หมายถึง วิธีทดสอบที่ผลการทดสอบไม่ขึ้นกับวิธีการที่กำหนดในวิธีทดสอบนั้น การใช้วิธีที่แตกต่างกัน จะให้ผลการทดสอบที่ไม่แตกต่างกัน และผลการทดสอบนี้สามารถสอบกลับได้ถึงหน่วยระบบสากล (SI unit)
- จำแนกตามปริมาณธาตุที่ทดสอบ แบ่งประเภทได้เป็น 3 วิธี ดังนี้
2.1 Impurity : Low concentration หมายถึง การทดสอบธาตุปริมาณต่ำ การทดสอบประเภทนี้ห้องปฏิบัติการต้องหาขีดจำกัดของการวัดเชิงปริมาณ (LOQ) โดยมีหลักฐานเป็นรูปธรรมที่แสดงปริมาณต่ำสุดที่แสดงความแม่น และความเที่ยง เป็นที่ยอมรับ
2.2 Limit test หมายถึง การทดสอบธาตุปริมาณต่ำมาก ๆ ซึ่งอาจมี หรือไม่มีธาตุนั้นในตัวอย่างก็ได้ การรายงานผลคือ ตรวจพบหรือไม่พบ การทดสอบประเภทนี้ต้องหาค่าขีดจำกัดของการตรวจวัด (LOD)
2.3 Major components: High concentration หมายถึงการทดสอบธาตุที่มีปริมาณความเข้มข้นสูงในตัวอย่าง ซึ่งห้องปฏิบัติการต้องตรวจสอบว่าความเข้มข้นที่สามารถทดสอบได้อยู่ระหว่างเท่าไร การทดสอบประเภทนี้ไม่จำเป็นต้องหาค่า LOD, LOQ
คุณลักษณะเฉพาะที่แสดงคุณสมบัติของวิธีที่สำคัญสำหรับ method validation ประกอบด้วย ความเลือกจำเพาะ (specificity), ความแม่น (accuracy), ความเที่ยง (precision), ขีดจำกัดของการตรวจวัด (detection limit; LOD), ขีดจำกัดของการวัดเชิงปริมาณ (quantitation limit; LOQ), สภาพไว (sensitivity), ช่วงการใช้งาน (working range), ความสัมพันธ์เชิงเส้นตรง (linearity), ความคงทน (robustness) และการกลับคืนของสารที่ทราบปริมาณ (recovery) โดยนิยามคำศัพท์ของ method validation ดังตารางที่ 1
ตารางที่ 1 นิยามคำศัพท์ของคุณลักษณะเฉพาะในการทำการตรวจสอบความใช้ได้ของวิธี (Belouafa et al., 2017)
| Validation characteristics | ICH definitions | |
| Specificity (ความเฉพาะเจาะจง) |
Specificity is the ability to assess unequivocally the analyte in the presence of components which may be expected to be present. Typically these might include impurities, degradants, matrix, etc. | ความสามารถของวิธีในการจำแนกสารที่สนใจวิเคราะห์ออกจากสารอื่นๆ รวมถึงสารปนเปื้อน สารที่เกิดจากการสลายตัวและเมทริกซ์ |
| Accuracy (ความแม่น) |
The accuracy of an analytical procedure expresses the closeness of agreement between the value that is accepted either as a conventional true value or an accepted reference value and the value found. This is sometimes termed trueness. | ความใกล้เคียงกันระหว่างค่าที่ได้จากการวิเคราะห์นั้น เปรียบเทียบกับค่าจริงหรือค่าอ้างอิงที่เป็นที่ยอมรับ |
| Precision (ความเที่ยง) |
The precision of an analytical procedure expresses the closeness of agreement (degree of scatter) between a series of measurements obtained from multiple sampling of the same homogenous sample under the prescribed conditions. Precision may be considered at three levels: repeatability, intermediate precision, and reproducibility. | ความใกล้เคียงกันระหว่างค่าที่ได้จากการวิเคราะห์ตัวอย่างเดียวกันซ้ำหลาย ๆ ครั้ง โดยตัวอย่างต้องเป็นเนื้อเดียวกัน ความเที่ยงแบ่งได้ 3 ระดับ คือ 1) repeatability 2) intermediate precision 3) reproducibility |
| 1) Repeatability expresses the precision under the same operating conditions over a short interval of time. Repeatability is also termed intra-assay precision. | 1) Repeatability คือการแสดงความเที่ยงของการวิเคราะห์ชุดการวิเคราะห์ซ้ำ ที่ทำในสภาวะเดียวกัน ในระยะเวลาที่ห่างกันไม่นาน | |
| 2) Intermediate precision expresses within-laboratories variations: different days, different analysts, different equipment, etc. | 2) Intermediate precision คือการแสดงความเที่ยงของการวิเคราะห์ชุดการวิเคราะห์ ที่ทำซ้ำ โดยมีการเปลี่ยนแปลงปัจจัยในการวิเคราะห์ในห้องปฏิบัติการเดียวกันเช่นเปลี่ยนเครื่องมือ เปลี่ยนผู้วิเคราะห์ เปลี่ยนวัน | |
| 3) Reproducibility expresses the precision between laboratories (collaborative studies usually applied to standardization of methodology). | การแสดงความเที่ยงของการวิเคราะห์ที่ทำโดยห้องปฏิบัติการหลายห้อง โดยทั่วไปใช้ในการนำเสนอวิธีใหม่ที่จะใช้เป็นวิธีมาตรฐาน | |
| Detection limit (ขีดจำกัดของการตรวจวัด) |
The detection limit of an individual analytical procedure is the lowest amount of analyte in a sample that can be detected but not necessarily quantitated as an exact value. | ปริมาณต่ำสุดของสารที่วิเคราะห์ในตัวอย่างใด ๆ ที่สามารถตรวจวัดได้ แต่ไม่จำเป็นต้องทราบว่ามีปริมาณที่แน่นอนเท่าใด |
| Quantitation limit (ขีดจำกัดของการวัดเชิงปริมาณ) |
The quantitation limit of an individual analytical procedure is the lowest amount of analyte in a sample that can be quantitatively determined with suitable precision and accuracy. The quantitation limit is a parameter of quantitative assays for low levels of compounds in sample matrices and is used particularly for the determination of impurities and/or degradation products. | ปริมาณต่ำสุดของสารที่วิเคราะห์ในตัวอย่างที่สามารถตรวจหาเชิงปริมาณโดยมีความถูกต้องและความเที่ยงอยู่ในเกณฑ์ที่เหมาะสม |
| Linearity (ความสัมพันธ์เชิงเส้นตรง) |
The linearity of an analytical procedure is its ability (within a given range) to obtain test results that are directly proportional to the concentration (amount) of analyte in the sample. | ความสามารถของวิธีที่จะทำให้วิเคราะห์แล้วได้ผลการวิเคราะห์ที่เป็นสัดส่วนกับความเข้มข้นของสารที่วิเคราะห์ในช่วงความเข้มข้นที่กำหนด |
| Working range (ช่วงการใช้งาน) |
The range of an analytical procedure is the interval between the upper and lower concentration (amounts) of analyte in the sample (including these concentrations) for which it has been demonstrated that the analytical procedure has a suitable level of precision, accuracy, and linearity. | ช่วงความเข้มข้นของสารที่จะวัดตั้งแต่ความเข้มข้นต่ำสุดถึงความเข้มข้นสูงสุดที่วัดแล้วมีความถูกต้อง ความเที่ยงและความสัมพันธ์เชิงเส้นตรงที่ยอมรับได้ |
| Robustness (ความคงทน) |
The robustness of an analytical procedure is a measure of its capacity to remain unaffected by small, but deliberate, variations in method parameters and also provides an indication of its reliability during normal usage. | ตัวชี้วัดให้เห็นถึงประสิทธิภาพของวิธีวิเคราะห์ว่ายังคงน่าเชื่อถือ แม้ว่าจะมีการเปลี่ยนแปลงตัวแปรบางอย่างในวิธีวิเคราะห์ |
ซึ่งการประเมินการตรวจสอบความใช้ได้ของวิธีไม่เป็นต้องทำครบทุกพารามิเตอร์ ซึ่งการทำพารามิเตอร์ใดบ้างขึ้นอยู่กับประเภทของวิธีวิเคราะห์ แนวทางการพิจารณาเลือกพารามิเตอร์ในการตรวจสอบความใช้ได้ของวิธี แสดงในตารางที่ 2
ตารางที่ 2 การแบ่งประเภทการทดสอบและคุณลักษณะเฉพาะของการตรวจสอบความใช้ได้ของวิธี (Chauhan, Mittu, & Chauhan, 2015)
| Performance characteristics (parameters) | Type of analytical procedure | |||
|---|---|---|---|---|
| Identification tests | Testing for impurities | Assay dissolution (measurement only) Content/potency | ||
| Quantitative | Limit | |||
| Accuracy | - | + | - | + |
| Precision | ||||
| Repeatability | - | + | - | + |
| Intermediate | - | + | - | + |
| Specificity | + | + | + | + |
| Detection limit | - | - | + | - |
| Quantitation limit | - | + | - | - |
| Linearity | - | + | - | + |
| Range | - | + | - | + |
| Robustness | + | + | + | + |
หมายเหตุ. เครื่องหมาย + เป็นพารามิเตอร์ที่ต้องทดสอบ และเครื่องหมาย - เป็นพารามิเตอร์ที่ไม่ต้องทดสอบ
คำศัพท์เฉพาะที่นิยมใช้ในการปฏิบัติของวิธีทดสอบและการทำการตรวจสอบความใช้ได้ของวิธีที่ควรรู้และทำความเข้าใจ เช่น
- Reagent blank คือ แบลงค์ที่ประกอบด้วยสารเคมีทุกชนิดที่ใช้ในทุกขั้นตอนการวิเคราะห์ โดยปราศจากสารที่สนใจ (analyte) เพื่อจะตรวจสอบว่าสารเคมีเหล่านั้นให้สัญญาณตอบสนองต่อเครื่องมือวัดหรือไม่
- Sample blank คือแบลงค์ที่เตรียมตามขั้นตอนการวิเคราะห์ทั้งหมดโดยมีตัวกลางของตัวอย่าง (matrix) รวมอยู่ด้วยแต่ปราศจากสารที่สนใจหรือมีในระดับต่ำๆ เพื่อตรวจสอบการรบกวนของสารที่ปนเปื้อนในตัวกลางของตัวอย่าง
- Fortified samples คือตัวอย่างที่เติมสารที่สนใจลงไปเพื่อเพิ่มสัญญาณจากสารที่สนใจและเพื่อศึกษาค่าการกลับคืน (recovery) การทำ fortify มักใช้กับการเติมสารที่สนใจเพิ่มลงไป
- Spiked samples คล้ายกับ fortify แต่การเติมสารมาตรฐานจะไม่จำกัดเฉพาะกับการเติมสารที่สนใจเท่านั้นแต่จะรวมถึงการเติมสารตัวอื่น ๆ เช่น internal standard, สารที่สงสัยว่าจะเป็นตัวรบกวนตัวอย่าง เป็นต้น
- Reference materials (RMs) วัสดุหรือสารที่มีคุณสมบัติหนึ่งอย่างหรือหลายอย่าง มีความเป็นเนื้อเดียวกันและเตรียมขึ้นอย่างดีเพื่อใช้สำหรับการสอบเทียบเครื่องมือ ใช้ในการประเมินวิธีวัดหรือใช้กำหนดค่าของวัสดุต่าง ๆ
- Certified reference materials (CRMs) วัสดุอ้างอิงที่มีใบประกาศรับรองค่าของคุณสมบัติอย่างหนึ่งหรือหลายอย่าง ผ่านการรับรองโดยวิธีการที่สามารถสอบกลับไปได้ยังค่าที่ถูกต้องที่แสดงไว้ พร้อมระบุค่าความไม่แน่นอนที่ระดับความเชื่อมั่นตามที่กำหนด
การตรวจสอบความใช้ได้ของวิธี ควรดำเนินการตามขั้นตอนดังนี้
1) เลือกวิธีทดสอบที่เหมาะสมกับประเภทตัวอย่างและปริมาณธาตุที่ต้องการทดสอบตามความต้องการของลูกค้าหรือเลือกจากวิธีที่ได้รับการยอมรับในกรณีที่ลูกค้าไม่ได้เจาะจงวิธีทดสอบ การเลือกวิธีทดสอบต้องพิจารณาดังนี้
1.1) วิธีมาตรฐานระดับนานาชาติ (International standard) เป็นมาตรฐานที่ได้จากข้อตกลงร่วมกันของประเทศสมาชิกต่าง ๆ ที่มีความสนใจร่วมกัน เช่นวิธีมาตรฐานของ ISO (International Standards Organization) ตัวอย่างเช่น
- ISO/TS 15495 | IDF/RM 230:2010, Milk, milk products and infant formulae – Guidelines for the quantitative determination of melamine and cyanuric acid by LC-MS/MS ใช้สำหรับการวิเคราะห์เชิงปริมาณของเมลามีนและกรดไซยานูริกในผลิตภัณฑ์นมสำหรับเด็กทารกโดยวิธี LC-MS/MS
1.2) วิธีมาตรฐานระดับภูมิภาค (Regional standard) เป็นมาตรฐานที่เกิดขึ้นจากการประชุมปรึกษาหารือกันระหว่างประเทศในภูมิภาคเดียวกัน แล้วกำหนดข้อตกลงร่วมกัน ส่วนมากจะเป็นการปรับมาตรฐานระดับประเทศในภูมิภาคเดียวกัน เช่น
- วิธีมาตรฐานของสหภาพยุโรป (European standard) หรือ European Norm (EN) ที่พัฒนาและเผยแพร่โดย European Committee for Standardization (CEN) หรือในภาษาฝรั่งเศสคือ Commite Europeen de Normalisation ตัวอย่างเช่น
- EN 1233:1996 Water quality - Determination of chromium - Atomic absorption spectrometric methods ใช้สำหรับการวิเคราะห์เชิงปริมาณของโครเมียมในน้ำโดยวิธีอะตอมมิกแอบซอร์บชันสเปกโทรเมตรี
- EN 14084:2003 Foodstuffs-Determination of trace elements - Determination of lead, cadmium, zinc, copper and iron by atomic absorption spectrometry (AAS) after microwave digestion ใช้สำหรับการวิเคราะห์เชิงปริมาณของของธาตุต่าง ๆ ในอาหาร
1.3) วิธีมาตรฐานระดับประเทศ (National standard) เป็นมาตรฐานที่ได้จากการประชุมหารือเพื่อหาข้อตกลงร่วมกันของผู้เกี่ยวข้องหลายฝ่ายในชาติ โดยมีหน่วยงานมาตรฐานของชาตินั้น ๆ เป็นศูนย์กลาง เช่น มาตรฐานผลิตภัณฑ์อุตสาหกรรม (มอก.) ของประเทศไทย ที่กำหนดโดยสำนักงานมาตรฐานผลิตภัณฑ์อุตสาหกรรม (สมอ.)
- มาตรฐานระดับประเทศที่ใช้กันอย่างกว้างขวาง ได้แก่ Japanese Industrial Standard (JIS) ของประเทศญี่ปุ่น และ British Standard (BS) ของสหราชอาณาจักร
- ประเทศสหรัฐอเมริกามีมาตรฐานระดับประเทศที่ยอมรับกันทั่วโลก ได้แก่
- The United States Environmental Protection Agency (USEPA)
- American Public Health Association (APHA)
- American Water Works Association (AWWA)
- National Institute for Occupational Safety and Health (NIOSH)
- Occupational Safety and Health Administration (OSHA)
1.4) มาตรฐานระดับสมาคม (Association standard) เป็นมาตรฐานที่กำหนดขึ้นจากกลุ่มบริษัทหรือโดยกลุ่มบุคคลที่อยู่ในวงการค้าเดียวกัน หรือเกิดจากข้อตกลงของกลุ่มบริษัทหรือโรงงานที่มีกิจกรรมของอุตสาหกรรมเป็นอย่างเดียวกัน หรือมีการผลิตของชนิดเดียวกัน ตัวอย่างเช่น
- American Association of Textile Chemists and Colorists (AATCC) เป็นสถาบันมาตรฐานของประเทศสหรัฐอเมริกาที่เกี่ยวกับการกำหนดมาตรฐาน การควบคุมคุณภาพมาตรฐานการทดสอบของวัสดุสิ่งทอและสีย้อมสิ่งทอที่ได้รับการยอมรับและนิยมใช้ทั่วโลก เช่น AATCC 112:2014 Formaldehyde Release from Fabric, Determination of: Sealed Jar Method
- มาตรฐานการทดสอบอุปกรณ์ไฟฟ้า เช่น ANSI/ESD STM11.13-2018 ESD Association Standard Test Method For The Protection of Electrostatic Discharge Susceptible Items - Two-Point Resistance Measurement เป็นต้น
1.5) วิธีมาตรฐานที่ตีพิมพ์โดยองค์กรทางวิชาการที่มีชื่อเสียงและเป็นที่ยอมรับ ในปัจจุบันมีหลายองค์กรที่เป็นที่ยอมรับในระดับนานาชาติ เช่น
- American Society for Testing and Materials (ASTM) ตัวอย่างเช่น ASTM F726-06 Standard Test Method for Sorbent Performance of Adsorbents
- Association of Official Analytical Chemists (AOAC) ตัวอย่างเช่น AOAC Official Method 999.10 Lead, Copper, Zinc and Iron in Foods: Atomic Absorption Spectrometry after Microwave Digestion
1.6) วิธีในตำราหรือวิธีที่ตีพิมพ์ในวารสารทางวิชาการที่เกี่ยวข้อง ตัวอย่างเช่น วิธีในตำราทางเคมีวิเคราะห์ Quantitative Chemical Analysis (9th Ed., 2015) โดย Harris สำหรับวารสารทางวิชาการที่เกี่ยวข้อง เช่น วารสารด้านเคมีวิเคราะห์ ได้แก่ Analytical Chemistry, Journal of Chromatography A, Analytica Chimica Acta, Food Chemistry, Analyst, Microchimica Acta และ Analytical Letters ตัวอย่างเช่น
- Visual and colorimetric detection of mercury(II) ion using gold nanoparticles Stabilized with a dithia-diaza ligand, Microchimica Acta, 2012, 176(1), 57-64. (Chansuvarn, & Imyim, 2012)
- Simple spectrophotometric method for determination of melamine in liquid milks based on green Mannich reaction. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy. 113(2013)154-158. (Chansuvarn, Panich, & Imyim, 2013)
วิธีทดสอบเหล่านี้ต้องได้รับการทวนสอบวิธีว่าสามารถดำเนินการได้ หากไม่มีมาตรฐานข้างต้นหรือไม่สามารถปฏิบัติตามได้ ห้องปฏิบัติการสามารถพัฒนาวิธีวิเคราะห์/วิธีทดสอบขึ้นเองได้ แต่ต้องทำ method validation ในพารามิเตอร์เหมาะสม
2) กำหนดวัตถุประสงค์ของวิธีทดสอบ เช่นเป็นการวิเคราะห์เชิงคุณภาพหรือปริมาณ ประเภทของสารที่สนใจ (analyte) ประเมินระดับความเข้มข้นของสารที่สนใจ พิจารณาเมทริกซ์จากตัวอย่าง องค์ประกอบทางกายภาพและเคมีอื่นที่เกี่ยวข้อง เป็นต้น
3) กำหนดเกณฑ์ที่ต้องการ (requirement) ในการทดสอบนั้น ซึ่งอาจกำหนดตามมาตรฐานที่กฎหมายกำหนด หรือตามวิธีมาตรฐานที่อ้างอิง หรือเกณฑ์กำหนดจากประสบการณ์ที่ผ่านมาหรือความสามารถของห้องปฏิบัติการ ประเภทวิธีทดสอบ ปริมาณธาตุที่ทดสอบ ช่วงความเข้มข้น และเนื้อสารของตัวอย่าง เกณฑ์กำหนดที่ชัดเจนสามารถนำไปเลือกคุณลักษณะเฉพาะที่แสดงคุณสมบัติของวิธีทดสอบได้อย่างถูกต้องและเหมาะสม
4) เลือกคุณลักษณะเฉพาะที่แสดงคุณสมบัติของวิธี (method performance characteristics) ต้องตรวจสอบ และกำหนดเกณฑ์การยอมรับและสถิติที่ใช้ในการตรวจสอบคุณลักษณะเฉพาะแต่ละตัว เช่น เกณฑ์การยอมรับความเที่ยง และความถูกต้อง เป็นต้น
5) กำหนดความต้องการทางเทคนิค เช่นสารเคมี เครื่องมือวิเคราะห์ สารมาตรฐาน เครื่องมือพื้นฐานที่ได้ผ่านการสอบเทียบแล้ว
6) จัดทำขั้นตอนการดำเนินการหรือคู่มือการปฏิบัติงาน (standard operation procedure) อย่างละเอียดและครบถ้วน
7) ดำเนินการตรวจสอบคุณลักษณะเฉพาะแต่ละตัวที่เลือกตามวิธีที่กำหนด
8) ตรวจสอบว่าเกณฑ์กำหนดต่าง ๆ สามารถบรรลุผลหรือไม่ เปรียบเทียบผลการทดสอบที่ได้กับเกณฑ์ที่กำหนดไว้ โดยใช้หลักสถิติช่วยในการตรวจสอบ หากผลการตรวจสอบไม่ผ่านเกณฑ์ อาจจำเป็นต้องตรวจสอบการใช้ได้ของวิธีใหม่ ปรับเปลี่ยนวิธีทดสอบ หรือปรับเกณฑ์กำหนด (ภาพที่ 1)
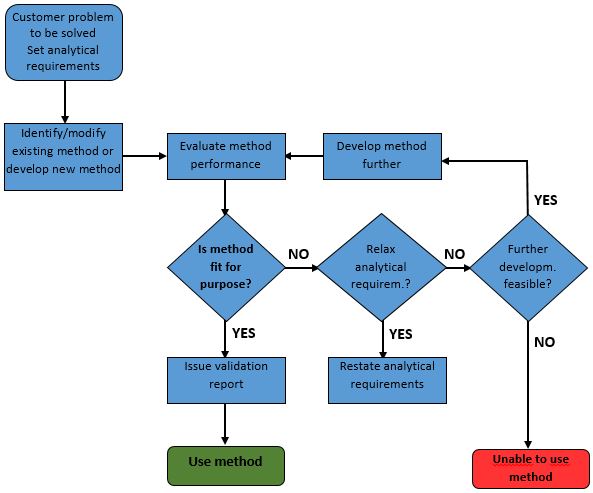
ภาพที่ 1 แสดงการเลือกวิธี การพัฒนาและประเมินวิธีทดสอบ (Magnusson et al.,2014)
9) สรุปผลว่าเป็นไปตามวัตถุประสงค์การใช้งาน เป็นข้อมูลที่ระบุว่าวิธีทดสอบได้มีการตรวจสอบความใช้ได้อย่างเหมาะสมและบรรลุวัตถุประสงค์ที่ตั้งไว้ คุณลักษณะเฉพาะของวิธีที่ต้องตรวจสอบจะต้องผ่านเกณฑ์ทุกองค์ประกอบที่ตรวจสอบ
- ผู้ตรวจสอบต้องมีความรู้ ความเข้าใจ และประสบการณ์ในงานนั้นเป็นอย่างดี และมีความรู้พื้นฐานทางสถิติที่ใช้ในการประเมินผล
- เครื่องมือจะต้องได้รับการสอบเทียบ หรือทวนสอบ เพื่อแสดงว่าสามารถให้ค่าความแม่น และความเที่ยงก่อนที่จะเริ่มตรวจสอบความใช้ได้ของวิธี
- เตรียมงบประมาณในการดำเนินการให้พร้อมสำหรับดำเนินการได้ครบถ้วนตามวัตถุประสงค์
- วัสดุที่ใช้ต้องมีความคงตัว เป็นเนื้อเดียวกัน มีเนื้อสารใกล้เคียงกับตัวอย่างที่ทดสอบประจำและมีปริมาณเพียงพอ ซึ่งผู้ตรวจสอบต้องเตรียมตัวอย่างควบคุม (Control sample) ให้เพียงพอสำหรับใช้งาน
- สารเคมีที่ใช้ควรเป็นเกรดวิเคราะห์ (Analytical reagent grade) ตามความเหมาะสมของแต่ละวิธี
- เตรียมจัดหาวัสดุอ้างอิงรับรอง (CRM) ไว้สำหรับการตรวจสอบความแม่นของวิธี ในกรณีที่วิธีวิเคราะห์นั้นสามารถใช้ CRM ในการตรวจวิเคราะห์ได้ (รายละเอียด CRM)
- มีการวางแผนการดำเนินการอย่างเหมาะสม รวมทั้งเตรียมความพร้อมของผู้ปฏิบัติงาน
เอกสารอ้างอิง
- วรวิทย์ จันทร์สุวรรณ. (2565). เคมีวิเคราะห์: หลักการและเทคนิคการคำนวณเชิงปริมาณ (พิมพ์ครั้งที่ 2). สำนักพิมพ์จุฬาลงกรณ์มหาวิทยาลัย.
- อภิชาติ อิ่มยิ้ม. (2559). การจัดทำระบบคุณภาพ ISO 17025 & GLP สำหรับห้องปฏิบัติการเคมี. สำนักพิมพ์จุฬาลงกรณ์มหาวิทยาลัย.
- AOAC. (2002). Appendix F: Guidelines for Standard Method Performance Requirements. http://www.eoma.aoac.org/app_f.pdf
- Belouafa, S., Habti, F., Benhar, S., Belafkih B., Tayane, S., Hamdouch, S., Bennamara, A., & Abourriche, A. (2017). Statistical tools and approaches to validate analytical methods: methodology and practical examples, Int. J. Metrol. Qual. Eng., 8, 1-10.
- Chansuvarn, W., & Imyim, A. (2012), Visual and colorimetric detection of mercury (II) ion using gold nanoparticles stabilized with a dithia-diaza ligand. Microchimica Acta. 176, 57-64.
- Chansuvarn, W., Panich, S., & Imyim, A. (2013). Simple spectrophotometric method for determination of melamine in liquid milks based on green Mannich reaction. Spectrochimica Acta A. 113, 154-158.
- Chauhan, A., Mittu, B., & Chauhan, P. (2015). Analytical Method Development and Validation: A Concise Review. J. Anal. Bioanal. Tech., 6, 1000233. https://doi.org/10.21276/IJPBS.2021.11.1.2
- Huber, L., 2007, Validation and Qualification in Analytical Laboratories, 2nd ed., Informa Healthcare USA, Inc.
- Magnusson, B., & Ornemark, U. (2014). Eurachem Guide: The Fitness for Purpose of Analytical Methods - A Laboratory Guide to Method Validation and Related Topics, 2nd ed., https://www.eurachem.org/index.php/mnu-tsk-mv
- Taverniers, I., Loose, M., & Bockstaele, E. V. (2004). Trends in quality in the analytical laboratory. II. Analytical method validation and quality assurance, TrAC Trends Anal. Chem., 23, 535-552.

